| Офіційне повне ім'я |
Рекомбінантний фактор некрозу пухлини людини-альфа/TNFSF2 GMP (rHuTNF-alpha/TNFSF2) |
| Послідовність |
 |
| Послідовність амінокислот |
MVRSSSRTPS DKPVAHVVAN PQAEGQLQWL NRRANALLAN GVELRDNQLV VPSEGLYLIY SQVLFKGQGC PSTHVLLTHT ISRIAVSYQT KVNLLSAIKS PCQRETPEGA EAKPWYEPIY LGGVFQLEKG DRLSFAEIG DRLFAEII |
| Синоніми |
Фактор некрозу пухлини, TNFSF2, кахектин, фактор, що індукує диференціацію, DIF, некрозин, цитотоксин |
| Номер вступу |
P01375 |
| GeneID |
7124 |
| Підсумки |
Фактор некрозу пухлини альфа (ФНП-альфа), також званий кахектином, є найбільш відомим членом сімейства ФНП, який може викликати загибель клітин. Цей білок продукується нейтрофілами, активованими лімфоцитами, макрофагами, NK-клітинами, LAK-клітинами, ендотеліальними клітинами астроцитів, клітинами гладкої мускулатури та деякими трансформованими клітинами. TNF-альфа зустрічається як секретована, розчинна форма і як закріплена на мембрані форма, обидва з яких є біологічно активними. Природна форма TNF-альфа є глікозильованою, але неглікозильований рекомбінантний TNF-альфа має порівнянну біологічну активність. Як повідомляється, біологічно активна нативна форма TNF-альфа є тримером. Людський і мишачий TNF-альфа демонструють приблизно 79 % гомології на рівні амінокислот і перехресну реакцію між двома видами. Було описано два типи рецепторів для TNF-альфа, і практично всі досліджені типи клітин показують наявність одного або обох цих типів рецепторів. |
| Source |
Кишкова паличка. |
| Молекулярна вага |
Приблизно 17.5 кДа, один неглікозильований поліпептидний ланцюг, що містить 158 амінокислот. |
| Біологічна активність |
Повністю біологічно активний у порівнянні зі стандартом. ED50, визначений за допомогою аналізу цитотоксичності з використанням мишачих клітин L929, становить менше 0.05 нг/мл, що відповідає специфічній активності > 2.0 × 107 МО/мг у присутності актиноміцину D. |
| Зовнішній вигляд |
Стерильний фільтрований білий ліофілізований (ліофілізований) порошок. |
| Формулювання |
Ліофілізований з 0.2 мкм фільтрованого концентрованого розчину в 10 мМ PB, 10 мМ NaCl, pH 7.0. |
| Ендотоксин |
Менше 0.01 ЄС/мкг rHuTNF-α/TNFSF2 GMP, як визначено методом LAL. |
| Відновлення |
Ми рекомендуємо цей флакон коротко центрифугувати перед відкриттям, щоб вміст опустився на дно. Розведіть у стерильній дистильованій воді або водному буфері, що містить 0.1 % BSA до концентрації 0.1-1.0 мг/мл. Матеріальні розчини слід розподілити на робочі аликвоти та зберігати при температурі ≤ -20 °C. Подальші розведення слід проводити у відповідних буферних розчинах. |
| Стабільність і зберігання |
Використовуйте морозильник з ручним розморожуванням і уникайте повторних циклів заморожування-розморожування.- Мінімум 12 місяців при зберіганні при температурі ≤ -20 °C у комплекті. Зверніться до специфічної сертифікації щодо дати використання.- 1 місяць, від 2 до 8 °C у стерильних умовах після розчинення.- 3 місяці, від -20 до -70 °C у стерильних умовах після відновлення. |
| посилання |
1. Davenport C, Kenny H, Ashley DT та ін. 2012. Eur J Clin Invest, 42: 1173-9.2. Cavalcanti YV, Brelaz MC, Neves JK та ін. 2012. Pulm Med, 2012: 745483.3. Sheng WS, Hu S, Ni HT та ін. 2005. J Leukoc Biol, 78: 1233-41.4. Berthold-Losleben MandHimmerich H. 2008. Curr Neuropharmacol, 6: 193-202. |
| SDS-PAGE |
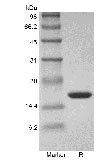 |
| Паспорт безпеки (SDS) Завантажити |
Натисніть, щоб завантажити |
| Технічний паспорт (TDS) Завантажити |
Натисніть, щоб завантажити |



