| Офіційне повне ім'я |
Фактор інгібування рекомбінантного лейкемії людини (rHuLIF) |
| Послідовність |
 |
| Послідовність амінокислот |
SPLPITPVNA TCAIRHPCHN NLMNQIRSQL AQLNGSANAL FILYYTAQGE PFPNNLDKLC GPNVTDFPPF HANGTEKAKL VELYRIVVYL GTSLGNITRD QKILNPSALS LHSKLNATAD ILRGLLSNVL CRLCDVSKYHVG HHSKLNATAD ILRGLLSNVL CRLCDVSKYHVG HHLFGDPYDVSKYHVG HSVKGFYKDVKGKLKGVKQGKGVKQGKDVKQKLKGVKQKG |
| Синоніми |
Фактор, що стимулює диференціацію, фактор D, інгібітор LPL, отриманий від меланоми, MLPLI |
| Номер вступу |
P15018 |
| GeneID |
3976 |
| Підсумки |
Фактор інгібування лейкемії (LIF) є членом сімейства інтерлейкінів 6. Цей білок в основному експресується в трофектодермі ембріона, що розвивається, а його рецептор LIFR експресується у всій внутрішній клітинній масі. LIF має здатність індукувати кінцеву диференціацію в лейкозних клітинах. Його діяльність включає індукцію диференціювання гемопоезу в клітинах нормальних і мієлоїдних лейкозів, індукцію диференціювання нейронних клітин і стимуляцію гострофазного синтезу білка в гепатоцитах. LIF використовується в культурі ембріональних стовбурових клітин миші, оскільки це видалення LIF штовхає стовбурові клітини до диференціювання, але вони зберігають свій проліферативний потенціал або плюрипотентність. Він також використовується у клінічних випробуваннях фази II, які можуть допомогти в імплантації ембріонів у жінок, які не змогли завагітніти, незважаючи на допоміжні репродуктивні технології (ДРТ). Зріла людська LIF (180 aa) має 78 %, 82 %, 91 %, 88 % та 87 % ідентичність послідовності aa з LIF миші, щура, собаки, великої рогатої худоби та свині, відповідно. |
| Source |
Кишкова паличка. |
| Молекулярна вага |
Приблизно 19.7 кДа, один неглікозильований поліпептидний ланцюг, що містить 180 амінокислот. |
| Біологічна активність |
Повністю біологічно активний у порівнянні зі стандартом. ED50, визначений за дозозалежною проліферацією клітин TF-1 людини, становить менше 0.1 нг/мл, що відповідає специфічній активності > 1.0 × 107 МО/мг. |
| Зовнішній вигляд |
Стерильний фільтрований білий ліофілізований (ліофілізований) порошок. |
| Формулювання |
Ліофілізований з 0.2 мкм фільтрованого концентрованого розчину в PBS, pH 7.4. |
| Ендотоксин |
Менше 1 ЄС/мкг rHuLIF, як визначено методом LAL. |
| Відновлення |
Ми рекомендуємо цей флакон коротко центрифугувати перед відкриттям, щоб вміст опустився на дно. Розведіть у стерильній дистильованій воді або водному буфері, що містить 0.1 % BSA до концентрації 0.1-0.2 мг/мл. Матеріальні розчини слід розподілити на робочі аликвоти та зберігати при температурі ≤ -20 °C. Подальші розведення слід проводити у відповідних буферних розчинах. |
| Стабільність і зберігання |
Використовуйте морозильник для ручного розморожування та уникайте повторних циклів заморожування-розморожування.- 12 місяців від дати отримання, від -20 до -70 °C у комплекті.- 1 місяць, від 2 до 8 °C у стерильних умовах після відновлення.- 3 місяці, Від -20 до -70 °C у стерильних умовах після розчинення. |
| посилання |
|
| SDS-PAGE |
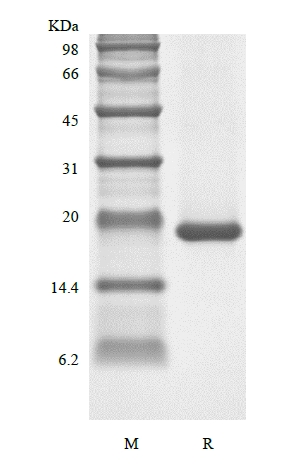 |
| Паспорт безпеки (SDS) Завантажити |
Натисніть, щоб завантажити |
| Технічний паспорт (TDS) Завантажити |
Натисніть, щоб завантажити |



