| Офіційне повне ім'я |
Рекомбінантний фактор росту кератиноцитів людини-2/FGF-10 (rHuKGF-2/FGF-10) |
| Послідовність |
 |
| Послідовність амінокислот |
LGQDMVSPEA TNSSSSSFSS PSSAGRHVRS YNHLQGDVRW RKLFSFTKYF LKIEKNGKVS GTKKENCPYS ILEITSVEIG VVAVKAINSN YYLAMNKKGK LYGSKEFNND CKLKERIEEN GYNTYASFNW QHNGRRKQMYVA LKIEKNGKVS GTKKENCPYS ILEITSVEIG VVAVKAINSN YYLAMNKKGK LYGSKEFNND CKLKERIEEN GYNTYASFNW QHNGRRKQMYVA HNGRRKQMYVA |
| Синоніми |
|
| Номер вступу |
O15520 |
| GeneID |
2255 |
| Підсумки |
|
| Source |
|
| Молекулярна вага |
Приблизно 19.1 кДа, один неглікозильований поліпептидний ланцюг, що містить 169 амінокислоту. |
| Біологічна активність |
Повністю біологічно активний у порівнянні зі стандартом. ED50, визначений за допомогою аналізу поглинання тимідину з використанням клітин BaF3, трансфікованих рецепторами FGF, становить менше 0.5 нг/мл, що відповідає специфічній активності > 2.0 × 106 МО/мг. |
| Зовнішній вигляд |
Стерильний фільтрований білий ліофілізований (ліофілізований) порошок. |
| Формулювання |
Ліофілізований з 0.2 мкм фільтрованого концентрованого розчину в 2 × PBS, pH 7.4. |
| Ендотоксин |
Менше 1 ЄС/мкг rHuKGF-2/FGF-10, як визначено методом LAL. |
| Відновлення |
Ми рекомендуємо цей флакон коротко центрифугувати перед відкриттям, щоб вміст опустився на дно. Розведіть у стерильній дистильованій воді або водному буфері, що містить 0.1 % BSA до концентрації 0.1-1.0 мг/мл. Матеріальні розчини слід розподілити на робочі аликвоти та зберігати при температурі ≤ -20 °C. Подальші розведення слід проводити у відповідних буферних розчинах. |
| Стабільність і зберігання |
Використовуйте морозильник для ручного розморожування та уникайте повторних циклів заморожування-розморожування.- 12 місяців від дати отримання, від -20 до -70 °C у комплекті.- 1 місяць, від 2 до 8 °C у стерильних умовах після відновлення.- 3 місяці, Від -20 до -70 °C у стерильних умовах після розчинення. |
| посилання |
1. Emoto H, Tagashira S, Mattei MG та ін. 1997. J Biol Chem. 272:23191-4.2. Tagashira S, Harada H, Katsumata T та ін. 1997. Ген. 197: 399-404.3. Карнінчі П, Касукава Т, Катаяма С та ін. 2005. Наук. 309:1559-63.4. Ігарасі М., Фінч П.В., Ааронсон С.А. 1998. J Biol Chem. 273:13230-5.5. Entesarian M, Matsson H, Klar J та ін. 2005. Nat Genet. 37:125-7. |
| SDS-PAGE |
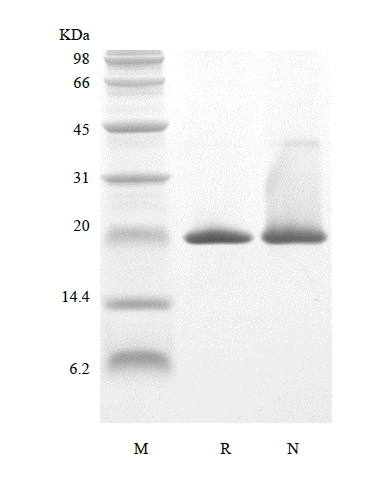 |
| Паспорт безпеки (SDS) Завантажити |
Натисніть, щоб завантажити |
| Технічний паспорт (TDS) Завантажити |
Натисніть, щоб завантажити |



